Диаграмма с эвтектикой
Обакомпонента неограниченно растворимы в жидком состоянии, ограниченно в твердом и не образуют химических соединений.
Компоненты: A,В.
Фазы: L, α,
β.
В сплавах такого рода возможно существование: жидкой
фазы, твердого раствора компонента Bв A, который мы будем называть α-раствором, и твердого
раствора компонентаАв В, который обозначим через β.
В этих сплавах возможно нонвариантное
равновесие при одновременном сосуществовании трех фаз: L, α,
β. В
зависимости от того, какая реакция протекает в условиях существования трех фаз, могут быть два вида
диаграмм: диаграмма с эвтектикой и диаграмма с перитектикой.
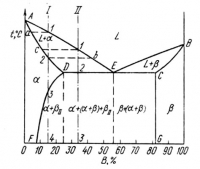
Диаграмма с эвтектикой
В этой системе не образуются фазы, представляющие собой чистые компоненты. Из жидкости могут выделяться только твердые растворыα или β. Следовательно, около вертикалейА и В , соответствующих чистым компонентам, находятся области существования твердых растворовα или β. Предельная растворимость компонентаВ в Аопределяется линиейDF,а предельная растворимостьА в В — линией CG.
Сплавы, находящиеся между этими двумя линиями, nbsp; находятся за пределами растворимости
двухфазными, состоящими из α + β. Окончание кристаллизации происходит по эвтектической реакции
L → α + β
Линия ЛЕВявляется на этой диаграммелинией ликвидус, линияADCB— линией, солидус. Зная правило фаз и правило отрезков, можно проследить за процессом кристаллизации любого сплава.
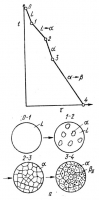
Кристаллизациясплава I . Выше точки1сплав находится в жидком состоянии. Вточке 1начинается процесс кристаллизации. Выделяются кристаллы твердого раствора а, концентрация которого изменяется по кривой а— 2, а состав жидкости изменяется по кривой 1 — b.Вточке 2кристаллизация закончится, и полученные кристаллы твердого раствора должны иметь (для равновесной кристаллизации) концентрацию исходной жидкости. Эти кристаллы не претерпевают изменений до точки 3, лежащей на линии предельной растворимости. Ниже этой точки твердый растворα является пересыщенным и выделяет избыточные кристаллы. Такими кристаллами являются кристаллыβ-твердого раствора, что определяют, применяя правило рычага для сплава, лежащего внутри двухфазной области α+β(т. е. для сплава ниже линииDF).
Состав твердого раствораα изменяется по кривой 3— F, вследствие выделениякристалловβконцентрации G.Количество кристалловβпри охлаждении увеличивается. Количество кристалловβ, выделившихся изсплава I, характеризуется отрезком от вертикалиIдо линии3—F.
Кривая охлажденияисхемы структур этого сплава при различных температурах показаны на рис.
Кристаллы β, выделившиеся из твердого раствора, называются вторичными кристалламии часто обозначаются символом βIIв отличие от первичных β-кристаллов (βI), выделяющихся из жидкости. процесс выделения вторичных кристаллов из твердой фазы носит название вторичной кристаллизациив отличие от процессапервичной кристаллизации, когда кристаллы (первичные) образуются в жидкой
фазе.
Нужно отметить, что сплав, концентрация которого лежит левее точкиF,не будет иметь вторичных выделенийβ-кристаллов.
Так как линияCGв отличие от линииFD изображена на рис. вертикальной, т. е. растворимость компонента Л в β не зависит от температуры, то вторичных выделенийα-кристаллов нет, но они были бы, если бы линияCGбыла наклонена вправо, т. е. растворимость уменьшалась бы с понижением температуры.
Точка Dдля твердого раствораα показывает максимальную растворимость компонентаВ в компонентеА при наиболее благоприятных условиях.
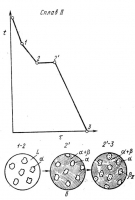
Кристаллизациясплава II. При кристаллизации этого сплава, в отличие от предыдущего, при достижении горизонтальной линииDECнаступает нонвариантная реакция. В равновесии находятся три фазы — жидкость E, α-кристаллы состава точкиDи β-кристаллы состава точки С. Индекс возле символа, обозначающего фазу, показывает состав фазы. Например, αDозначает твердый растворα состава точкиD.По достижении температуры, соответствующей горизонтали DEC,наступает
эвтектическая реакция — из жидкости выделяются кристаллы обоих твердых растворов:
LE→αD+βC
Реакция эта нонвариантна, так как при двух компонентах в реакции участвуют три фазы (с = к — f + +1=2-3+1=0).
Все три фазы, участвующие в реакции, имеют определенные составы (проекции точек E, Dи С) и температура их превращения постоянна.
В результате кристаллизации сплава II, кроме первичных (выделившихся при охлаждении от точки 1 до точки2)кристаллов а, образуется еще эвтектикаα + β.
При дальнейшем охлаждении вследствие изменения растворимостиα-кристаллы выделяют вторичные кристаллыβIIи при нормальной температуреα-кристаллы (как первичные, так и входящие в эвтектику) будут иметь состав, отвечающий точкеF.
Кривая охлаждения сплаваII и структуры этого сплава показаны на рис.
Выделение вторичных кристаллов из эвтектических составляющих обычно не обнаруживается при микроскопическом исследовании, так как вторичные выделения объединяются с такой же (одноименной) фазой эвтектики.
Несмотря на многообразие структурных составляющих окончательно охлажденный сплав содержит только две фазы α и β, и правило фаз, если его применить ниже линииDEпокажет все количество α- и β-фаз независимо от того, в какой структурной форме они находятся.
- Источники:
- Диаграммы состояния двойных и многокомпонентных систем на основе железа. Банных О. А., Будберг П.Б., Алисова С. П. и др. Металлургия, 1986 г.
- Двойные и многокомпонентные системы на основе меди. под ред. Шухардина С.В. Наука, 1979 г.
- Диаграммы состояния двойных металлических систем ред. Лякишева Н.П.Машиностроение, 1996-2000 г.