Диаграмма с перитектикой
Оба компонента неограниченно растворимы в жидком состоянии, ограниченно в твердом и не образуют химических соединений.
Компоненты: A,В.
Фазы: L, α,
β.
В сплавах такого рода возможно существование: жидкой
фазы, твердого раствора компонента B в A, который мы будем называть α-раствором, и твердого
раствора компонента Ав В, который обозначим через β.
В этих сплавах возможно нонвариантное
равновесие при одновременном сосуществовании трех фаз: L, α,
β. В
зависимости от того, какая реакция протекает в условиях существования трех фаз, могут быть два вида
диаграмм: диаграмма с эвтектикой и диаграмма с перитектикой.
Диаграмма с перитектикой
При эвтектическом превращении жидкость кристаллизуется с образованием двух твердых фаз. Возможен и другой тип нонвариантного превращения (трехфазного равновесия), когда жидкость реагирует с ранее выпавшими кристаллами и образует новый вид кристаллов L+β→α
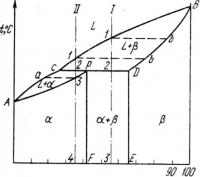
Реакция подобного типа называется перитектической. Диаграмма с перитектическим превращением показана на рис. На диаграмме показаны три однофазные области: жидкость L и ограниченные твердые растворы α и β.
Линия ABCявляется линией ликвидус, линия APDB— линией солидус.
Кристаллизациясплава I. Кристаллизация начинается в точке 1 , когда из жидкости выпадают кристаллы β-раствора состава точки b. Затем по мере снижения температуры жидкость меняет свою концентрацию по линии ликвидус от точки 1 до точки С, а кристаллы β — по линии солидус от точки bдо точки D. По достижении перитектической горизонтали CPD состав жидкости будет отвечать точке С, а состав кристаллов — точке D. Эти обе фазы реагируют и дают третью фазу а, концентрация которой определяется точкой Ρ — третьей точкой на горизонтали. Перитектическая реакция изображается следующим образом:
LC+βD→αP или в более общем случае L+β→αтак как точки Dи Ρ показывают предельную концентрацию твердых растворов β и α (для простоты линии предельной растворимости даны вертикальными). Количественное соотношение фаз при перитектической реакции, необходимое для образования α-фазы, определяется по правилу отрезков соотношением
Количество β = CP Количество L=PD
В рассматриваемом же сплаве количество участвующих в перитектической реакции кристаллов β и жидкости определяется соотношением
Количество
β = C2
Количество L= 2D
т. е. в данном сплаве имеется избыток β-фазы по сравнению с тем количеством, которое необходимо для образования α-кристаллов. Поэтому по окончании реакции в избытке остаются β-кристаллы. Следовательно, в структуре будут продукты перитектической реакции (т. е. α-кристаллы) и оставшиеся избыточные первичные β-кристаллы. Чем ближе точка 2 лежит к точке P, тем меньше в реакции остается избыточных β-кристаллов.
Для сплава, отвечающего по концентрации точке Р, соотношение реагирующих при перитектическом превращении жидкости и β-кристаллов таково, что оно как раз достаточно для образования α-кристаллов предельной концентрации.
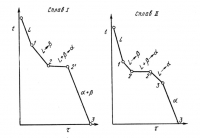
На рис. а показана кривая охлаждения сплава I. Для перитектической кристаллизации (средняя схема) характерно то, что новая α-фаза появляется на границе реагирующей друг с другом жидкости и β-кристаллов. Для сплава I перитектической реакцией заканчивается процесс кристаллизации.
Кристаллизациясплава II (рис. б). Отличие кристаллизации этого сплава от кристаллизации сплава I состоит в том, что при перитектической температуре имеется избыток жидкой фазы по сравнению с тем количеством, которое необходимо для образования α-кристаллов концентрации Р. Поэтому перитектическое превращение заканчивается исчерпанием β-твердого раствора, и оставшаяся жидкость в интервале между точками 2'— 3 кристаллизуется в α-фазу. При этом концентрация жидкости изменяется по кривой С—а, а концентрация образующихся α-кристаллов — по Ρ — 3 .
- Источники:
- Диаграммы состояния двойных и многокомпонентных систем на основе железа. Банных О. А., Будберг П.Б., Алисова С. П. и др. Металлургия, 1986 г.
- Двойные и многокомпонентные системы на основе меди. под ред. Шухардина С.В. Наука, 1979 г.
- Диаграммы состояния двойных металлических систем ред. Лякишева Н.П.Машиностроение, 1996-2000 г.